|
| 조현주 IBS 바이오분자 및 세포 구조 연구단 차세대연구리뎌.[IBS 제공] |
[헤럴드경제=구본혁 기자] 기초과학연구원(IBS) 바이오분자 및 세포 구조 연구단 조현주 차세대연구리더 연구팀은 김호민 KAIST 생명과학과 교수, 이성배 DGIST 뇌과학과 교수 연구팀과 함께 단백질 공학을 이용해 퇴행성 신경질환인 헌팅턴병에 효과적인 치료용 샤페론을 개발했다고 20일 밝혔다.
헌팅턴병은 유전적 돌연변이에 의해 헌팅틴 단백질 유전자에 CAG 반복서열이 비정상적으로 증가해 발생한다. CAG 반복서열의 증가는 헌팅틴 단백질의 급격한 응집을 유발해 독성 응집체를 형성하고, 신경세포 내에 축적되면서 세포 기능을 방해해 결국 신경세포 사멸을 초래한다. 보통 30~40대에 진행이 시작돼 비자발적이고 제어되지 않은 움직임, 발음장애, 연하곤란 , 인지장애 등의 증상이 나타나며, 합병증이나 신체 기능의 저하로 사망에 이를 수 있다. 그러나 아직 근본적 치료제를 찾지 못했으며, 증상 완화를 위한 약물 치료에 그치고 있다.
연구진은 세포 내 단백질 항상성 유지에 핵심인 ‘샤페론(Chaperone)’에 주목했다. 샤페론은 세포 내에서 단백질이 3차원으로 올바로 접히도록 하고, 잘못 접힌 단백질의 응집을 방지해 단백질이 제 기능을 할 수 있게 돕는다. 먼저 연구진은 막단백질 샤페론 중 하나인 PEX19에 무작위 돌연변이를 유도해 수십만 개의 변이 라이브러리를 제작했다. 그리고 이를 이용해 만든 변이체들을 효모 독성 기반 스크리닝 기법으로 선별해 헌팅틴 단백질의 독성을 억제하는 변이 샤페론 PEX19-FV를 개발했다.
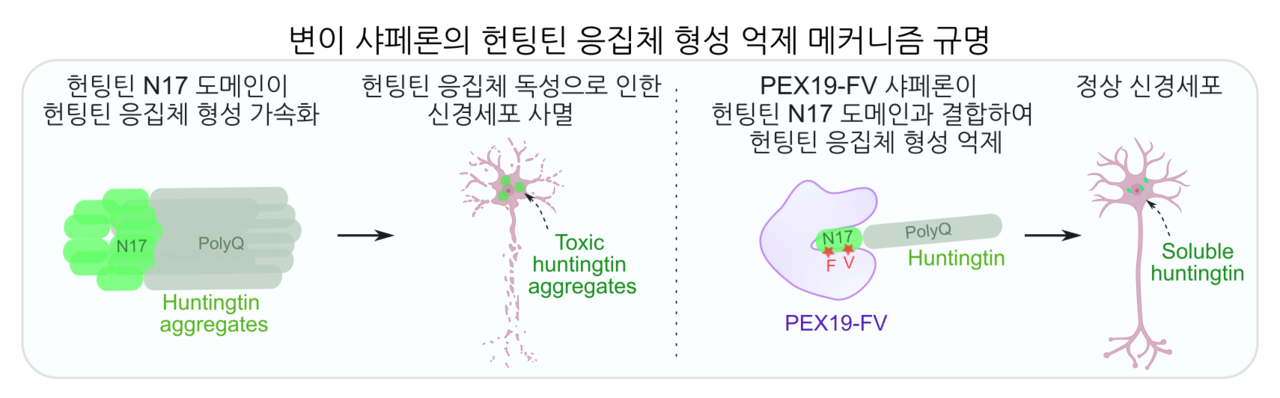 |
| 변이 샤페론의 헌팅틴 응집체 형성 억제 메커니즘 규명.[IBS 제공] |
PEX19-FV는 변형된 소수성 잔기를 통해 헌팅틴 단백질의 소수성 부위와 결합하고 헌팅틴 단백질 간 상호작용을 차단했다. 이를 통해 헌팅틴 단백질의 응집을 효과적으로 억제하고 독성 응집체 축적을 막았다.
이어 동물 및 세포 실험을 통해 PEX19-FV의 효과를 확인했다. 헌팅틴 단백질이 과발현돼 신경 퇴행 증상을 보이는 초파리에 PEX19-FV를 발현시키자, 시험관 벽을 기어오르는 능력이 약 2배 향상되며 운동 능력이 크게 개선됐다. 또한 초파리의 평균 생존율이 약 3배 증가하는 놀라운 결과를 보였다. 나아가, 생쥐 뇌에서 추출한 신경세포를 배양해 헌팅틴 단백질과 함께 PEX19-FV를 발현시킨 결과, 약 80%에 달하던 신경세포의 심각한 구조적 손상이 5% 이하로 감소하고, 신경세포의 사멸도 약 10배 줄어드는 효과를 보였다.
조현주 차세대연구리더는는 “이번 연구로 개발한 변이 샤페론은 헌팅틴 단백질의 응집을 효과적으로 억제해 신경세포를 보호할 수 있다”며 “기존 샤페론을 적절히 변형시켜 헌팅턴병뿐만 아니라 다양한 퇴행성 신경질환 치료도 가능할 것”이라고 말했다.
이번 연구 결과는 국제학술지 ‘네이처 커뮤니케이션즈’에 1월 17일 온라인 게재됐다.