중남미 시장 첫 개별 국가 진출 성과
항생제 무사용 공정으로 안전성 확보
항생제 무사용 공정으로 안전성 확보
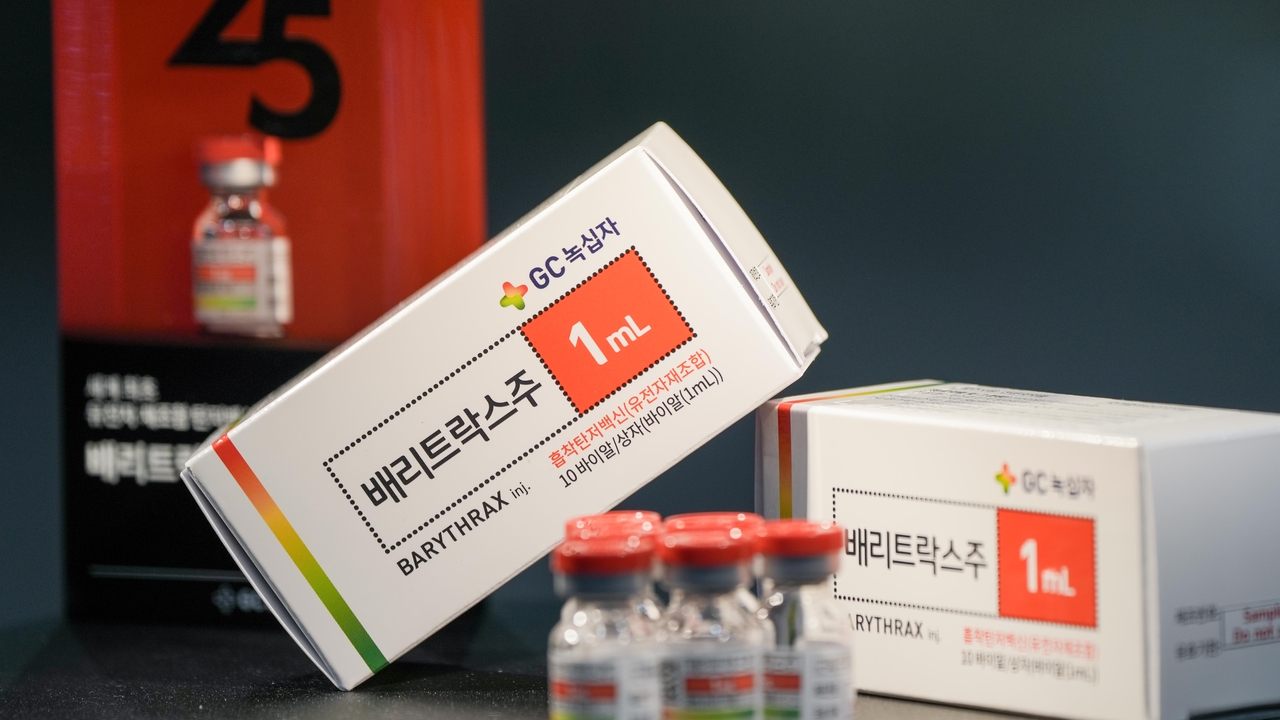 |
| 세계 최초 유전자 재조합 단백질 탄저백신 ‘배리트락스주’. 28년의 연구개발 끝에 8일 국내에 첫 출하됐다. [질병관리청 제공] |
[헤럴드경제=최은지 기자] GC녹십자는 자사의 수두백신 ‘배리셀라주’가 과테말라 공중보건사회복지부로부터 품목허가를 획득했다고 26일 밝혔다.
배리셀라주가 중남미 국가에서 품목허가를 받은 것은 이번이 처음이다. 회사는 기존 범미보건기구(PAHO)를 통한 공급망에 더해, 이번 허가를 기점으로 중남미 개별 국가로의 시장 확장을 가속화한다는 방침이다.
배리셀라주는 GC녹십자가 독자 개발한 ‘MAV/06’ 균주를 사용한 생백신이다. 특히 제조 공정에서 카나마이신, 네오마이신, 에리트로마이신 등 항생제를 전혀 사용하지 않는 세계 최초의 수두백신으로 개발됐다. 이를 통해 항생제 잔류물로 인한 이상반응 가능성을 차단하고 제품 안전성을 높였다는 평가다.
백신의 면역원성 지표도 우수한 것으로 나타났다. 장기 추적 임상 결과에 따르면 접종 후 체내 중화항체 생성 비율은 99~100%를 기록했다. 항체 지속성 또한 글로벌 선도 제품과 대등한 수준임을 입증했다.
최근에는 세계보건기구(WHO) 권고안(Position paper)에 등재되면서 Oka 균주 기반의 글로벌 백신과 동등한 국제적 평가를 받게 됐다. 이에 따라 글로벌 시장 내 교차 처방도 가능해져 활용 범위가 넓어질 전망이다.
이재우 GC녹십자 개발본부장은 “이번 허가는 중남미 첫 품목허가라는 점에서 의미가 깊다”며 “차별화된 제품력을 바탕으로 배리셀라주의 글로벌 입지를 높여갈 것”이라고 말했다.